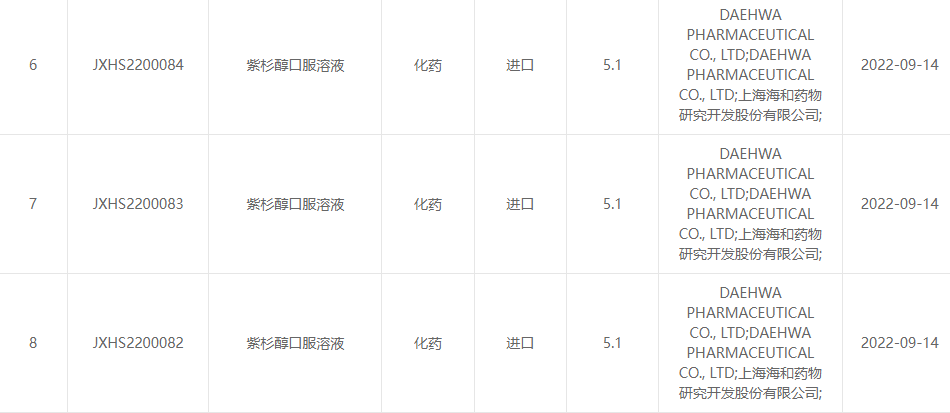
13. septembra 2022 sta družbi Shanghai Haihe Pharmaceutical Research and Development Co., Ltd. in Daehwa Pharmaceutical Co., Ltd. skupaj objavili, da je Center za zdravila uradno odobril peroralno raztopino paklitaksela (RMX3001), ki sta jo skupaj razvili obe strani. Ocena (CDE) Državne uprave za zdravila.(Številka sprejema: država JXHS2200082, država JXHS2200083, država JXHS2200084).
Vir slike: Državna uprava za zdravila
paklitakselse pogosto uporablja pri zdravljenju različnih malignih tumorjev, kot so pljučni rak, rak dojke, rak jajčnikov, rak glave in vratu ter rak želodca.Polimerizacija beljakovin, sestavljanje mikrotubulov, preprečevanje depolimerizacije, s čimer se stabilizirajo mikrotubule in zavira mitoza rakavih celic ter sproži apoptoza, s čimer se učinkovito preprečuje proliferacija rakavih celic in igra učinek proti raku.
Trenutno večina delov sveta uporablja paklitaksel v obliki injekcije, ki jo je treba oblikovati in aplicirati z intravensko kapljanjem v bolnišnici.Bolniki se morajo pogosto vračati v bolnišnico, na mestu injiciranja pa se bodo pojavili neželeni učinki.Zato je bil razvoj peroralnih pripravkov paklitaksela vedno vroča točka v industrijskih raziskavah..
RMX3001 je peroralna formulacija paklitaksela, ki jo je razvila družba Dahua Pharmaceutical na podlagi svoje inovativne tehnologije dostave zdravil, ki samoemulgira lipide.Septembra 2016 ga je odobrila Korejska uprava za hrano in zdravila (trgovsko ime Liporaxel), indikacija pa je napredovalo ali zdravljenje druge izbire metastatskega raka želodca ali lokalno ponavljajočega se raka želodca.Glede na sporočilo za javnost Haihe Pharmaceuticals je Liporaxel prvi peroralni izdelek paklitaksela, ki je bil doslej uspešno razvit in odobren za trženje v svetu.Septembra 2017 je Haihe Pharmaceutical od Dahua Pharmaceuticals pridobil pravice za raziskave in razvoj, proizvodnjo in prodajo izdelka na celinski Kitajski, v Hongkongu, Tajvanu in na Tajskem.
Prijava RMX3001 na seznam na Kitajskem temelji predvsem na randomiziranem, odprtem, vzporedno nadzorovanem, neinferiornem načrtu, večcentričnem kliničnem preskušanju 3. faze, katerega namen je primerjati drugo linijo zdravljenja s peroralno raztopino paklitaksela RMX3001 in injekcija paklitaksela (Taxol) Učinkovitost in varnost pri bolnikih z napredovalim rakom želodca.Študijo sta kot glavna raziskovalca skupaj izvedla profesor Li Jin iz šanghajske orientalske bolnišnice in profesor Qin Shukui iz bolnišnice Nanjing Jinling.
Dr. Ruiping Dong, glavni izvršni direktor Haihe Pharmaceuticals, je dejal: »Sprejetje vloge za peroralno raztopino paklitaksela (RMX3001) je še en pomemben mejnik za Haihe Pharmaceuticals in zelo sem hvaležen kliničnim raziskovalcem in bolnikom, ki so sodelovali v našem sojenje.Napredovali rak želodca Še vedno obstaja velika neizpolnjena klinična potreba po zdravljenju in upamo, da bomo bolnikom na Kitajskem in po svetu čim prej zagotovili najsodobnejšo inovativno in priročno zdravljenje na svetu.«
Yunnan Hande Biotechnology Co., Ltd. se že 28 let osredotoča na proizvodnjo paklitaksela.Je prvi neodvisni proizvajalec rastlinskega zdravila proti raku paklitaksela na svetu, ki so ga odobrili ameriški FDA, evropski EDQM, avstralski TGA, kitajski CFDA, Indija, Japonska in druge nacionalne regulativne agencije.podjetje.Če želite kupitiPaclitaxel API,kontaktirajte nas prek spleta.
Čas objave: 14. septembra 2022